先天性肾上腺皮质增生症
先天性肾上腺皮质增生症是一组常染色体隐性遗传病,由于肾上腺皮质类固醇激素合成过程中某种酶的先天缺陷,引起肾上腺皮质激素合成不足,经负反馈作用促使下丘脑、垂体分泌促肾上腺皮质激素释放激素和促肾上腺皮质激素增加,导致肾上腺皮质增生和代谢紊乱。临床主要表现为不同程度的肾上腺皮质功能减退、性腺发育异常、伴或不伴水盐代谢紊乱与高血压,以糖和盐皮质激素替代治疗为主,疗效和预后取决于酶缺陷的程度、就诊的早晚及开始治疗的早晚 患者的依从性,能否坚持服药和定期随诊等。
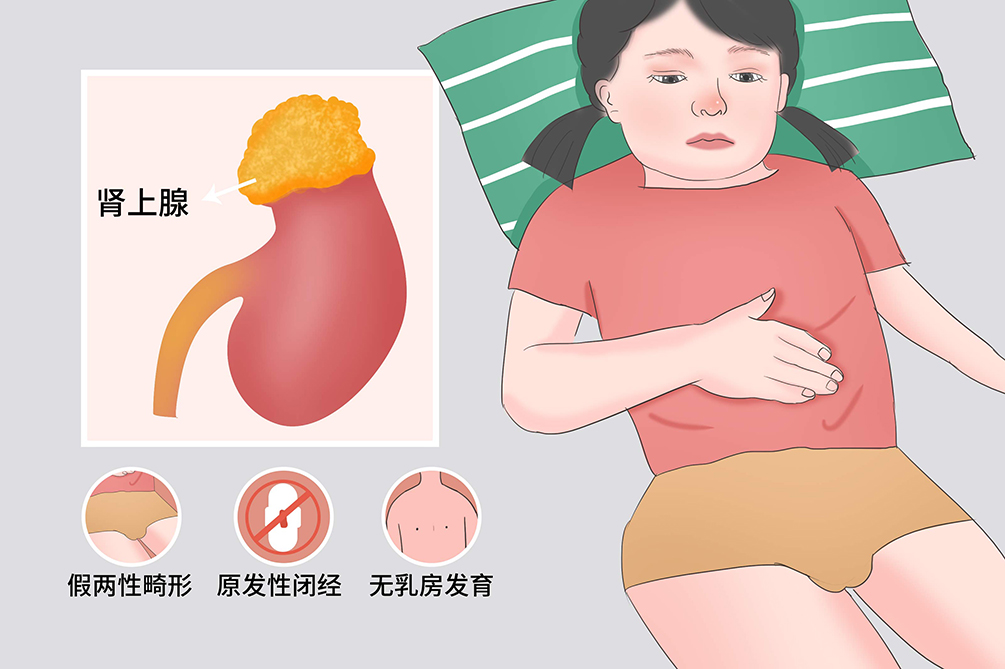
先天性肾上腺皮质增生症的病因主要包括21-羟化酶缺乏症、11β-羟化酶缺乏症、3β-羟脱氢酶缺乏症、17α-羟化酶缺乏症、胆固醇碳裂解酶缺乏症、类脂性肾上腺增生症等类型。其中21-羟化酶缺乏症最常见,约占总数的 90%~95% , 11β-羟化酶缺乏症次之,约占 7%,再其次为3β-羟脱氢酶缺乏症,17α-羟化酶缺乏症和胆固醇碳裂解酶缺乏症则十分罕见。
主要病因21-羟化酶缺乏
为最常见的一种类型,约占先天性肾上腺皮质增生症患者的90%~95%。该酶的缺陷使最终产物皮质醇和盐皮质激素产生不足和17羟孕酮的堆积,伴雄激素分泌过多。
11β-羟化酶缺乏
为第二种常见类型,约占5%~8%。由于CYP11β基因突变,肾上腺不能进一步合成皮质醇,11-去氧皮质醇增多和11-去氧皮质酮、脱氢异雄酮和4-雄烯二酮分泌增多,引起女性男性化和男性假性性早熟。
17α-羟化酶缺乏
是较少见的类型 、占本病的1%。CYP17缺陷使肾上腺、睾丸、卵巢的性激素的合成完全被阻断。
3β-羟脱氢酶缺乏
是一种危险的类型,皮质醇和盐皮质激素合成均严重受阻。
细胞色素P450氧化还原酶缺乏
是一种罕见的先天性肾上腺皮质增生症,由于细胞色素P450氧化还原酶缺陷,导致类固醇激素合成障碍。
先天性类脂质性肾上腺增生
是最少见和最严重的一型,肾上腺皮质不能合成皮质醇、醛固酮及雄激素等任何一种皮质激素,胆固醇不能被利用,而在细胞内存积。垂体促肾上腺皮质激素促进皮质增生,表现为类脂质细胞的增生。
诱发因素近亲婚配:本病为常染色体隐性遗传,近亲婚配使得该病患病率增加。
胃肠疾病、感染、围手术、疼痛、心理压力、药物不足、突发事故等易诱发肾上腺危象。
流行病学本病是较常见的常染色体隐性遗传病,发病常有家族性,在同一家族中常表现为同一类型的缺陷。典型的先天性肾上腺皮质增生症发病约为1/10000 ~1/ 20000活产新生儿,同种族先天性肾上腺皮质增生症发病也有很大区别。
好发人群本病为较常见的常染色体隐性遗传病,因此发病常有家族性,在同一家族中常表现为同一类型的缺陷。
症状先天性肾上腺皮质增生症以女孩多见,男女之比约为1: 2,其临床表现取决于酶缺陷的部位及缺陷的严重程度。
典型症状21-羟化酶缺乏症
典型失盐型
呕吐、腹泻、喂养困难、体重不增、脱水、酸中毒及难以纠正的低血钠、高血钾等表现,多在生后1~2周发病。新生儿出生后即可表现为肾上腺危象,如不及时治疗,可出现血容量降低、血压下降和休克。
单纯男性化
女性胎儿外生殖器男性化,女性男性化的程度不一,可从单纯阴蒂增大常被误认为男性化不全的男性,到完全性阴囊性尿道下裂伴隐睾的男性。若不及时治疗阴蒂可继续增大,体毛增多,痤疮出现,女性第二性征发育不良,甚至无乳房发育和原发性闭经,无生殖能力。男性患儿出生时外生殖器可无明显异常,易误诊。随生长过程因高雄激素作用,在婴幼儿期,阴茎进一步增大,睾丸不大,伴有或不伴有阴毛早现的外周性性早熟,由于性激素过早、长时期的作用,使儿童期生长过速伴骨龄快速增长,骨骺过早闭合致成人矮身材。
非典型的晚发型
大多出生时无临床症状,外生殖器正常,随年龄增长女性患者可有阴毛早现,月经初潮延迟,月经量过少或部分患者可发生严重痤疮,不明原因的骨骺成熟增速 、生长增快的表现,最后身高矮于父母的平均身高。
11β-羟化酶缺乏症
典型
部分出现高血钠、低血钾、碱中毒和高血容量,又可因皮质醇减少出现皮质功能减低的症状及雄激素过高的症状。
非典型
非典型者临床差异较大,大部分因面部痤疮、月经不调来就诊,少数有高血压,大多血压正常。
17α-羟化酶缺乏症
大部分患儿出现高血压、高血钠、低血钾和碱中毒,有轻度皮质醇不足的症状,男性假两性畸形,男性女性化。女性因雌激素缺乏表现性幼稚至青春发育期无第二性征发育,原发闭经。
3β-羟脱氢酶缺乏症
出生时即可出现失盐和肾上腺皮质功能不全症状,严重者因循环衰竭而死亡。男性为不同程度的外生殖器发育不全,如小阴茎,女性不同程度男性化、多毛、月经不调。
并发症肾上腺危象
是一种威胁生命的突发状况,典型临床表现是脱水、低血压、低钠血症、高钾血症、低血糖或精神症状。若不治疗或治疗不及时,高钾血症会导致猝死。
甲状腺功能减退
先天性肾上腺皮质增生症患者中观察到的低血糖、低血压、智力发育迟缓及心血管风险增加可能与甲状腺激素的作用有关,但目前尚未查阅到明确的关于先天性肾上腺皮质增生症与甲状腺功能减退症之间的关系。
心肌损害
糖皮质激素不足可能在心肌损害中起一定作用,糖皮质激素的缺乏会导致心脏功能差、对儿茶酚胺的血管反应差,以及抗利尿激素分泌增加。
就医此病可用糖和盐皮质激素替代治疗,预防肾上腺危象发生。维持正常生长和骨骼成熟,力求达到理想的终身高。对家庭和患儿不良心理进行疏导。
就医指征对家族中有本病先证者的孕妇应做羊水细胞或者取绒毛膜进行产前基因诊断。
新生儿出生后第3天~5天,测定足跟血17-0HP 水平,筛查先天性肾上腺皮质增生症,已经确诊者应积极治疗并定时随访与监测。
就诊科室大多患者优先考虑去儿科、儿童内分泌科、遗传病专科就诊。
医生询问病情因为什么来就诊的?
有无早筛?
目前都有什么症状?(如阴唇肥大、多毛、闭经等)
以前是否有其他内分泌科诊治经历?
既往有无其他的病史?
需要做的检查尿液17-羟类固醇 、17-酮类固醇和孕三醇测定:17-酮类固醇是反映肾上腺皮质分泌雄激素的重要指标,对本病的诊断价值优于17-羟类固醇。肾上腺皮质增生症患者17-酮类固醇明显升高。
血17-羟孕酮、肾素血管紧张素原、醛固酮、脱氢表雄酮、去氧皮质酮及睾酮测定血17-羟孕酮、孕酮、脱氢表雄酮、睾酮均可增高,其中血17-羟孕酮增高可为正常的几十倍至几百倍,是21-羟化酶缺乏症较可靠的诊断依据。
血皮质醇、促肾上腺皮质激素测定:典型失盐型先天性肾上腺皮质增生症患者的皮质醇水平低于正常,单纯男性化可在正常范围或稍低于正常。血促肾上腺皮质激素不同程度升高,部分患儿尤其非典型者可正常。
血电解质:失盐型可有低血钠、高钾血症。
染色体检查:外生殖器严重畸形时,可进行染色体分析,以鉴定性别。
X线检查:拍摄左手腕掌指骨正位片,判断骨龄,患者骨龄常超过年龄。
CT、MRI检查:可发现双侧肾上腺增大。
基因诊断:采用直接聚合酶链反应、寡核苷酸杂交、限制性内切酶片段长度多态性和基因序列分析可发现相关基因突变或缺失。
诊断标准对于假两性畸形、失盐症群、高血压或低血压、低血钾和碱中毒表现的患者,均应考虑本病。
影像学检查对肾上腺肿瘤有定位诊断价值:B 超发现双侧肾上腺回声增强、增宽,则应进一步检查。CT和MRI检查表现为双侧肾上腺影普遍增大,边缘略呈结节状,但仍保持其大体形态,结构正常。
对胎儿或新生儿进行产前诊断可以CYP21缺陷症为目标,在怀孕后第2个3月期间进行。在第1个3月期,妊娠期9周或以后的绒毛膜活检采样,第2个3月期诊断以怀孕第 14周或以后行羊膜腔穿刺术。
新生儿筛查主要用于典型CYP21D缺陷症的筛查,测定出生24 h后足跟血液中 17-OHP,如升高可诊断70%的典型CYP21D缺陷症。
鉴别诊断先天性肥厚性幽门狭窄症
表现为特征性的喷射性呕吐,钡剂造影可发现狭窄的幽门,无皮肤色素沉着,外生殖器正常。失盐型易误诊为先天性肥厚性幽门狭窄或肠炎,故如遇新生儿反复呕吐、腹泻,应注意家族史、生殖器外形等,必要时进行相关检查。
真性性早熟
单纯男性化型睾丸容积与实际年龄相称,17-酮类固醇明显升高,而真性性早熟睾丸明显增大,17-酮类固醇增高,但不超过成人期水平。
男性化肾上腺肿瘤
男性化肾上腺肿瘤和单纯男性化型均有男性化表现,尿17-酮类固醇均升高,需进行地塞米松抑制试验,男性化肾上腺肿瘤不被抑制,而单纯男性化型则显示较小剂量地塞米松即可显著抑制。
治疗先天性肾上腺皮质增生症治疗原则为纠正水、电解质紊乱,儿童首选氢化可的松或醋酸氢化可的松,有失盐者需补充盐皮质激素,药物剂量应个体化,应激情况应加大肾上腺皮质激素药物剂量。女性患者及失盐型男女患者应终生治疗,单纯男性化型的男性患者在进入青春期和成年期后可酌情停药,必要时切除增生的肾上腺。
治疗周期 先天性肾上腺皮质增生症需要进行长期持续性治疗。 急症治疗肾上腺危象治疗
纠正脱水,纠正低血钠,补充生理盐水,必要时补充3%高张钠,9α-氟氢可的松口服、氢化可的松静滴,一周后减量,3~4周后减至维持量。纠正严重高血钾,如高血钾难以纠正可予葡萄糖加胰岛素静滴。
应激状态治疗
因感染发热,体温高于38.5℃时腹泻伴有脱水、严重外伤、全麻手术,导致肾上腺衰竭的疾病等,增加皮质醇的剂量,轻度感染增加1~2倍,重度感染增加2~5倍,并同时控制感染。可以达到正常人在应激状态时皮质醇增加的浓度,病情好转后需迅速减回至维持治疗用量。
药物治疗皮质醇替代治疗:采用氢化可的松或醋酸氢化可的松治疗,补充肾上腺分泌皮质醇不足同时抑制垂体促肾上腺皮质激素的分泌,从而使雄激素的产生减少并阻止男性化的继续发展,发挥正常生长潜能。糖皮质激素剂量应根据生长速率、骨成熟度、17-羟孕酮、睾酮、促肾上腺皮质激素等指标调整。
盐皮质激素治疗:9α-氟氢可的松可协同糖皮质激素作用,使促肾上腺皮质激素分泌进一步减少。
肾上腺皮质增生症时伴有肾上腺结节性腺瘤可考虑手术切除部分增生的肾上腺,后期肾上腺激素水平低可进行相应激素替代治疗。
手术治疗阴蒂退缩成形术
女孩阴蒂增大,需手术治疗,最适宜手术年龄为2岁前,术前最好进行染色体核型的检查,以确定遗传性别。
阴道成形术
严重者需早期进行外生殖器矫形手术,应向家长说明在月经来潮之前还应确定阴道是否有先天畸形。
其他治疗当治疗过程中出现真性性早熟,骨龄明显超速时,可联合应用促性腺激素释放激素治疗,抑制中枢性性早熟,争取骨骺晚闭合,尽量达到理想的终身高。
预后先天性肾上腺皮质增生的患儿治疗得当,两性均可有正常的青春发育和生育功能。
能否治愈本病大多需终身治疗,单纯男性化的男性患者进入青春期或成人,可适当停药动态观察。
能活多久治疗得当一般不会影响自然寿命。
复诊经过治疗的患者应根据年龄和开始治疗后的反应,开始需要每1~2月一次,剂量调整好后可3~6个月复查一次。
饮食先天性肾上腺皮质增生症患儿需食用富含维生素及高热量的食物,失盐型患儿每日的钠摄入量不少于10 克~20 克,多喝水,维持身体水分。对于拒食的患儿需耐心喂养,必要时候可利用滴管或者鼻饲来满足患儿的生理需要。
饮食调理宜补充足量的鱼肉蛋白维生素等,满足身体基本需要。
对于婴幼儿,注意及时添加辅食,可以添加少量多餐配方奶。
护理先天性肾上腺皮质增生症患者需要加强饮食管理,积极预防感染,预防肾上腺危象,积极进行心理干预与治疗。
日常护理在激素应用过程中,应注意观察激素的副作用,按时服用护胃药、补钙药等。不要轻易停药减药,在发生应激性事件例如感染、手术等情况时,应遵医嘱适量调整激素用药。
注意保暖,保持患儿全身皮肤干燥清洁,同时加强对患儿的口腔护理,勤剪指甲,保持房内干净、通风。
特殊注意事项观察患儿精神情况,有无脱水、厌食、呕吐、头痛、嗜睡等不适,一旦发生肾上腺危象,立即就医。
当患儿出现呕吐症状时,需抱住患儿头部向前倾,用手扶住患儿的前额头,让呕吐物吐出,以免呕吐物进入呼吸道而引发窒息情况。
预防先天性肾上腺皮质增生症是常染色体隐性遗传病,预防措施包括新生儿筛查和产前诊断。
预防措施新生儿筛查
主要对21-羟化酶缺乏症筛查,目的是避免和预防延迟诊断治疗造成的肾上腺皮质危象而导致的死亡。过多雄激素造成患儿日后身材矮小、心理生理发育异常。
产前诊断
先天性肾上腺皮质增生症是常染色体隐性遗传病,每生育一胎就有1/4概率为先天性肾上腺皮质增生症患者。因此,对家族中有本病先证者的孕妇应做羊水细胞或者取绒毛膜进行产前基因诊断。
参考文献
[1]江载芳,申昆玲,沈颖.诸福棠实用儿科学[M].北京:人民卫生出版社,2014.
[2]桂永浩,薛新东.儿科学[M].北京:人民卫生出版社,2015.
[3]王卫平,孙锟,常立文.儿科学[M].北京:人民卫生出版社,2018.
[4]王唯,任艳类.类固醇21-羟化酶缺乏导致的先天性肾上腺皮质增生症2018年新版指南解读[A].西部医学,2019.
[5]陈晓红.肾上腺皮质功能不全与代谢危象及猝死[A].中国实用儿科杂志,2019.
[6]李强,郭琳.先天性肾上腺皮质增生症的诊断与处理[A].内科急危重症杂志, 2016.
[7]叶青.先天性肾上腺皮质增生症临床病例分析[D].新疆医科大学,2019.
[8]刘倩,黎雪梅,杨权春.儿童先天性肾上腺皮质增生症的临床护理对策分析[J].世界最新医学信息文摘,2019.
[9]曲晓瑜,金昌沫.探讨先天性肾上腺皮质增生症患儿的临床护理方法[J].世界最新医学信息文摘,2016.
本文出处:https://jk.yebaike.cn/view/253.html

 微信扫一扫
微信扫一扫